Оптическая спектрометрия с внедрением эффекта плазмонного резонанса позволяет учить белки, владеющие оптической плотностью в видимом спектре электрического излучения (хромопротеины) при помощи измерения поглощения света на определённых («характеристических» для определенных молекул) длинах волн. Но для таких измерений требуются достаточно высочайшие концентрации белкá, ну и пространственное разрешение этого способа очень низкое (обычно изучают смеси молекул, находящиеся в спектрометрических кюветах, и речи о том, где конкретно в клеточке размещены изучаемые молекулы, просто не идёт).
Еще большей чувствительностью владеют способы, основанные на измерении флуоресценции. Совместно с конфокальной микроскопией они позволяют определять месторасположение молекул с внутри живой клеточки, но здесь нужно видоизменять изучаемые молекулы особыми молекулами-метками, что не всегда лучше и может быть.
Другой нередко применяемый в биологии способ — спектроскопия ядерного магнитного резонанса — также просит достаточно огромных концентраций белка и нередко — изотопного мечения объекта, сложного в критериях живых систем.
Методика с внедрением плазмонного резонанса базирована на внедрении в живы клеточки микрочастиц металла определенного размера (20–30 нм). При всем этом электроны на поверхности частиц из таких металлов как золото либо серебро коллективно осциллируют в ответ на облучение светом определённой длины волны. Резонансные частоты этих микрочастиц зарегистрировать намного легче, чем слабенький (из-за очень низких концентраций) оптический сигнал от био молекул, что и позволяет проводить измерения.
Измерения основаны на явлении, именуемом миграцией энергии плазмонного резонанса(МЭПР), которое состоит в том, что молекулы белка, адсорбирующиеся на поверхности золотых частиц, вроде бы «оттягивают» на себя часть энергии плазмонного резонанса, что довольно просто зарегистрировать по специфичным «провалам» в диапазонах рассеяния, «снимаемых» с этих частиц.
Основным условием этого эффекта является перекрывание частоты плазмонного резонанса и частот оптического поглощения белка, — требование, аналогичное тому, которое накладывается и в более обширно известном способе резонансного переноса энергии флуоресценции. Конкретно этим условием и определяется то, что частички состоят из золота, и их размер определяет пик плазмонного резонанса в области 530–580 нм, перекрывая спектр поглощения цитохрома (с), который был избран для исследования.
В установке, приведенной на рисунке 12.5, микрочастицы золота освещаются под определённым углом через фазовоконтрастный конденсор. Изучаемым параметром является светорассеяние (на величину которого как раз и оказывает влияние плазмонный резонанс), регистрируемое цветной камерой и анализируемое при помощи спектрофотометра.
«Тушение» плазмонно-резонансного диапазона, обусловленное миграцией энергии на адсорбирующиеся на поверхности микрочастиц биомолекулы, проявляется в виде специфичных «провалов» на диапазонах рассеяния в спектрах длин волн, совпадающих с пиками оптического поглощения молекул белка (рис. 1.17 г). Для действенного переноса энергии нужно, чтоб диапазоны рассеяния и поглощения перекрывались. Так как такая резонансная миграция является прямым переносом, и, как следует, происходит резвее и эффективнее, чем оптическое поглощение, диапазоны МЭПР могут быть зарегистрированы обычной оптической системой, что было бы нереально при использовании «обычной» оптической спектроскопии.
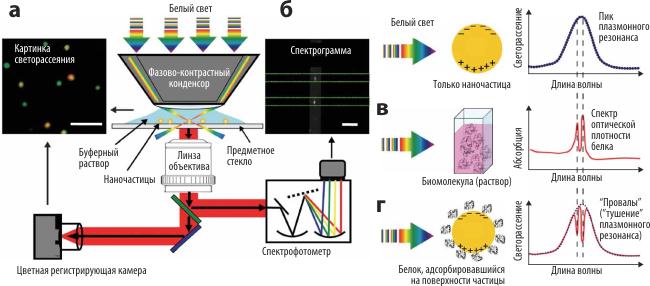

Рис. 1.17 Явление «тушения» плазмонного резонанса вследствие передвижения энергии на биомолекулы. А. Схема установки. Б. Обычный диапазон рэлеевского (упругого) рассеяния микрочастиц золота. В. Обычный диапазон оптического поглощения белка.
Соответствующие пики и провалы на приведенных графиках (Г): для окисленной формы Fe III (530 нм); для восстановленной Fe II (525 нм и 550 нм); провалы на диапазоне плазмонного резонанса (рассеяния) вызваны миграцией энергии на биомолекулу в спектрах длин волн, соответственных пикам оптического поглощения белкá.
Для исследовательских работ не непременно использовать конкретно золото: подобные опыты были проведены и на серебряных микрочастицах, взаимодействующих с гемоглобином. Если же использовать другие металлы, то можно учить аналогичный эффект в ультрафиолетовой либо ближней инфракрасной областях диапазона, к примеру, чтоб идентифицировать взаимодействие с нуклеиновыми кислотами либо большинством белков, не всасывающих свет в видимой области.
Исследователи считают, что более многообещающая область использования нового способа (беря во внимание его беспримерную чувствительность и возможность внедрения в живой клеточке) — это генетический анализ молекул РНК и товаров экспрессии генов, изредка включающихся в «нормальных» критериях и про работу которых практически ничего не понятно. Не считая того, можно будет определять белки-спутники разных форм рака, токсины и вирусные частички.
